|
|
供應(yīng) 【技術(shù)轉(zhuǎn)讓】芬戈莫德原料+膠囊(化3+3)臨床批件 /162359-56-0  |
規(guī) 格: |
硬膠囊�����,0.5mg |
價(jià) 格: |
面議/元/公斤 |
數(shù) 量: |
1 |
交貨地: |
山東濟(jì)南 |
發(fā)布時(shí)間: |
2018-01-27 |
有效期: |
255天 |
備 注: |
【藥品名稱】芬戈莫德(Fingolimod)
【CAS】162359-56-0
【注冊(cè)分類】化藥3.1類
【劑型及規(guī)格】硬膠囊����, 0.5 mg
【適應(yīng)癥】復(fù)發(fā)-緩解型多發(fā)性硬化癥(MS)
【項(xiàng)目簡(jiǎn)介】
芬戈莫德(Fingolimod)是由日本M itsubishi制藥公司研發(fā)��, 后期全球經(jīng)營權(quán)轉(zhuǎn)讓給瑞士Novartis制藥公司����, 2010 年9月21日獲得美國FDA批準(zhǔn)上市, 成為首個(gè)可經(jīng)口服給藥的用于治療復(fù)發(fā)緩解型多發(fā)性硬化癥(multiplesclerosis�����,MS)的新型免疫抑制劑,商品名為:Gilenya.可以阻止淋巴腺中的部分血細(xì)胞向大腦和脊髓移動(dòng)���,從而延緩多發(fā)性硬化癥患者的病情惡化程度�����。-+
目前用于多發(fā)性硬化癥的主要藥物為:那他珠單抗�、β-干擾素����、鹽酸米托蒽醌、格拉默等����,但是這些藥物多采用長時(shí)程的腸道外給藥模式,既增加了患者的負(fù)擔(dān)����,又減少了藥物應(yīng)用的依從性。并且不能長效抑制病情��,必需頻繁注射給藥,還會(huì)引發(fā)一些副作用�,如流感樣副作用及注射部位炎癥反應(yīng)等。
芬戈莫德為首個(gè)防止淋巴細(xì)胞從淋巴結(jié)中離開的鞘氨醇1-磷酸鹽受體調(diào)節(jié)劑類藥���,降低多發(fā)性硬化癥患者疾病復(fù)發(fā)的頻率���,延緩多發(fā)性硬化癥患者的病情惡化程度。它還可以保持淋巴結(jié)內(nèi)特定的免疫細(xì)胞���,防止它們作用于中樞神經(jīng)系統(tǒng)并造成損害���,并且對(duì)淋巴細(xì)胞的保持力是可逆的,從而使患者在治療停止后體內(nèi)循環(huán)的淋巴細(xì)胞恢復(fù)到正常水平����。
全球目前80億美元的多發(fā)性硬化癥藥物市場(chǎng)隨著新藥的上市,還具有翻一番的增長空間����,其中最具決定性的因素就是注射劑型向口服劑型的轉(zhuǎn)變。芬戈莫德的主要對(duì)手——默克公司克拉屈濱片(cladribine����,Movectro)的申請(qǐng)?jiān)?011年4月遭到FDA拒絕���,而在2月的時(shí)候,默克主動(dòng)撤回了Movectro在歐洲的藥品上市許可申請(qǐng)�。芬戈莫德是神經(jīng)鞘氨醇1-磷酸受體調(diào)節(jié)劑的新類藥物的首個(gè)獲批產(chǎn)品��,目前國內(nèi)尚無注冊(cè)受理�����,將會(huì)擁有巨大的銷售市場(chǎng)�。
【專利及保護(hù)】無化合物專利,有工藝專利�����。
【進(jìn)展情況】已申報(bào)臨床��,國內(nèi)第5家申報(bào) |
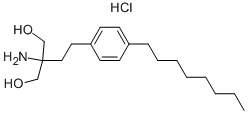
結(jié)構(gòu)式: |
 |
|
|

