|
|
供應(yīng) 瑞戈非尼(化藥3+4�,技術(shù)轉(zhuǎn)讓,不賣產(chǎn)品) /11  |
規(guī) 格: |
片劑���。100mg���;150mg |
價(jià) 格: |
面議/ |
數(shù) 量: |
1 |
交貨地: |
山東濟(jì)南 |
發(fā)布時(shí)間: |
2018-01-27 |
有效期: |
255天 |
備 注: |
【項(xiàng)目名稱】瑞戈非尼(化藥3+4����,技術(shù)轉(zhuǎn)讓,不賣產(chǎn)品)
【商品名稱】Stivarga
【規(guī) 格】片劑���,0.4g
【適 應(yīng) 癥】
(1)治療既往接受過氟尿嘧啶�、奧沙利鉑和伊立替康為基礎(chǔ)的化療�����,以及既往接受過或不適合接受抗VEGF治療��、抗EGFR治療(RAS野生型)的轉(zhuǎn)移性結(jié)直腸癌患者��;
(2)治療既往接受過甲磺酸伊馬替尼及蘋果酸舒尼替尼治療的局部晚期的���、無法手術(shù)切除的或轉(zhuǎn)移性的胃腸間質(zhì)瘤患者;
(3)治療既往接受過索拉非尼治療的肝細(xì)胞肝癌(2017.04 FDA新增的適應(yīng)癥)���。
【項(xiàng)目簡介】
瑞戈非尼(Regorafenib,商品名:Stivarga)于2011年由拜耳和美國生技制藥公司聯(lián)合開發(fā)���,于2012年9月27日,F(xiàn)DA批準(zhǔn)用于治療轉(zhuǎn)移性結(jié)直腸癌(CRC)患者�����。2013年2月28日FDA批準(zhǔn)瑞戈非尼(Stivarga®)片劑用于治療先前接受過伊馬替尼和舒尼替尼治療的局部晚期,不能手術(shù)切除或轉(zhuǎn)移性胃腸道間質(zhì)瘤(GIST)患者�。2013年8月26日EMA批準(zhǔn)上市瑞戈非尼用于轉(zhuǎn)移性結(jié)直腸癌、2014年7月EMA再次批準(zhǔn)用于胃腸道間質(zhì)瘤���。2013年3月25日��,PADA批準(zhǔn)用于轉(zhuǎn)移性結(jié)直腸癌����,8月20日再次批準(zhǔn)用于胃腸道間質(zhì)瘤�,2017.04新增的適應(yīng)癥是治療既往接受過索拉非尼治療的肝細(xì)胞肝癌。
結(jié)直腸癌是胃腸道中常見的惡性腫瘤��,早期癥狀不明顯�,隨著癌腫的增大而表現(xiàn)排便習(xí)慣改變、便血�、腹瀉、腹瀉與便秘交替�、局部腹痛等癥狀,晚期則出現(xiàn)貧血��、體重減輕等全身癥狀�����。其發(fā)病率和病死率在消化系統(tǒng)惡性腫瘤中僅次于胃癌、食管癌和原發(fā)性肝癌�����。中國在世界上屬于低發(fā)地區(qū)����,但其發(fā)生率在不少地區(qū)有程度不等的增加趨勢(shì)。
專家估計(jì)2013年結(jié)直腸癌藥物在美國�,歐洲5國(法國,德國��,意大利����,西班牙和英國),日本和中國的市場銷售額為50.2億美元�����,美國作為最大的結(jié)直腸癌藥品市場銷售額22.3億(45%)����,其后5個(gè)歐洲地區(qū)銷售額17.1(34%)���,日本和中國市場占比最小�,分別為8.17億(16%)和2.59億(5%)。
截至至2023年�,預(yù)測(cè)這八個(gè)地區(qū)結(jié)直腸癌藥物市場銷售額增至81.1億元,年復(fù)合增長率4.9%���。特別提出�����,預(yù)計(jì)中國結(jié)直腸癌藥物市場將快速增長�,至2023年銷售額為10.5億����,年復(fù)合增長率為15.1%。此外�����,至2023年雖然所有地區(qū)市場均有增長�,但美國和日本的市場占比分別減至40%和13%,5個(gè)歐洲地區(qū)維持在34%���。
【國內(nèi)生產(chǎn)及研制情況】 原研片劑已獲得SFDA批準(zhǔn)在中國上市����,規(guī)格為:0.4g。
【知識(shí)產(chǎn)權(quán)情況】本品化合物專利CN1856469A��,到期日2024.7.22��。
【進(jìn)度】已獲臨床批件�����,尋求廠家合作?���,F(xiàn)計(jì)劃按照化藥3+4類申報(bào),其他抗腫瘤或者其他優(yōu)質(zhì)品種技術(shù)合作����,歡迎有意向企業(yè)來電垂詢。18854188208 |
結(jié)構(gòu)式: |
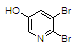 |
|
|